Класификации
Класификация на сърдечната недостатъчност (HF) според фракцията на изтласкване на лявата камера (LVEF)
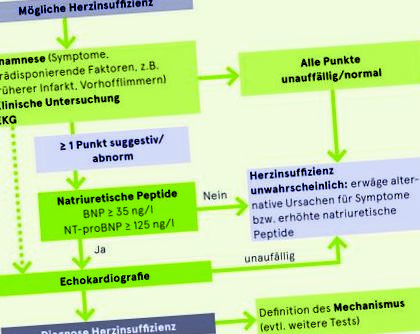
Диагнозата на сърдечната недостатъчност се основава на следните критерии:
Клиничният отговор на терапията подкрепя диагнозата, но сам по себе си е недостатъчен за диагнозата.
Алгоритъмът (съгласно Насоките на ESC от 2016 г.) основно се прилага както за остра, така и за неостра или хронична обстановка. Показаната тук версия е за пациенти с хронични симптоми. Разграничението е важно, тъй като се прилагат различни гранични стойности за B-тип натриуретични пептиди (BNP) и N-терминал-proBNP (NT-proBNP). Пределните граници от 35 и 125 ng/l, предложени за не-острата настройка, са много ниски и имат висока отрицателна прогнозна стойност (изключване). Има различни несърдечни причини за повишени стойности на BNP и NT-proBNP (табл. Страница). Трябва също да се отбележи, че BNP и NT-proBNP са неспецифични количествени маркери на сърдечния (особено лявокамерния) стрес и не могат да предоставят никаква информация за механизма. Следователно винаги ще е необходима ехокардиография, за да се потвърди диагнозата и да се илюстрира механизмът на сърдечната недостатъчност.
В настройки с лесен достъп до ехокардиография (като в Швейцария) е възможно да се премине директно към ехокардиография без определяне на BNP/NT-pro (пунктирана линия). В острата среда граничните стойности за BNP и NT-proBNP са съответно 100 и 300 ng/l. Тези граници имат висока отрицателна прогнозна стойност за изключване на сърдечна недостатъчност при пациенти с остра диспнея. Стойностите над границата не са категорични за сърдечна недостатъчност дори при остри условия и трябва да доведат до допълнителни тестове (предимно ехокардиография). За повече информация относно диагностичната процедура при остри условия вижте "Остра сърдечна недостатъчност".
- Предимно остра декомпенсация на хроничен процес
- Декомпенсация на хронична сърдечна недостатъчност с ограничена помпена функция поради задействане (вижте «Причини/причини за остра декомпенсация» страница)
- Декомпенсация в случай на сърдечна недостатъчност със запазена функция на помпата, т.е. д. Обикновено в резултат на хипертонично дерайлиране и/или обемно претоварване ("остра сърдечно-съдова недостатъчност")
- Редки остри процеси (миокарден инфаркт, аритмия, миокардит, остра клапна недостатъчност и др.)
Остра сърдечна недостатъчност (AHF) = потенциално животозастрашаващо състояние, което изисква бързо и систематично действие. Диагностичен и терапевтичен подход съгласно фиг. 2. Идеята на този подход е да се пристъпи към диференциална диагноза и да се предприемат мерки за спасяване на живота веднага паралелно.
Причини/причини за остра декомпенсация
- Миокардна исхемия/инфаркт
- Неадекватна терапия/несъответствие
- Съпътстващи лекарства (НСПВС, включително COX-2 инхибитори, стероиди, трициклични антидепресанти, литий, блокери на калциевите канали)
- Бъбречна недостатъчност
- Недостатъчен прием на вода/сол
- Аритмии (особено тахикардно предсърдно мъждене)
- Прогресия на витиум на клапата
- инфекция
- Белодробна емболия
- Хипертиреоидизъм, анемия
- Токсини, кардиодепресанти
терапия
Причинна терапия, когато е възможно и възможно най-рано (вж. Фиг. 2 „Насоки на ESC 2016“), в противен случай/допълнително поддържаща терапия според клиничния и хемодинамичния профил. Тази терапия е по същество емпирична (прогностичният ефект на тези мерки не е доказан). Целта е бързо подобряване на симптомите и клинична стабилизация, за да може да се установи терапията на хронична сърдечна недостатъчност. Тъй като оптималната терапевтична стратегия за остра сърдечна недостатъчност е неизвестна, важно е колкото се може повече пациенти да бъдат включени в подходящи проучвания въпреки спешната ситуация. В зависимост от степента на тежест, лечението се извършва в спешно отделение/нормално отделение или спешно отделение/MIPS, вероятно с инвазивно наблюдение. Според състоянието на хидратация („мокра или суха“) и тъканна перфузия („топла или студена“, не винаги, но често синоним на нормотоничен срещу хипотоничен), могат да се разграничат четири хемодинамични профила, които осигуряват грубата посока на терапията по смисъла на първоначална концепция.
- „Влажно и топло“ (по-голямата част от пациентите): нормално или хипертонично и претоварено: спешна терапия с CPAP/NIV, вазодилататори
- „Мокро и студено“: неблагоприятно, хипотонично и претоварено: спешна терапия с CPAP/NIV, инотропи, вазопресори; Пещера: помислете за интубация/вентилация и механична поддръжка рано
- "Сухо и топло": относително благоприятна ситуация, адаптиране на оралната терапия
- "Сухо и студено": предимно заместване на обема; реакцията на това определя по-нататъшната процедура
Решението „мокър“ или „сух“ се подкрепя от ултразвук, когато е възможно (В-линии, интраваскуларно и сърдечно пълнене и др.), Както и решението за прилагане на титриран обем (250–500 ml всеки) или прилагане на диуретици по време на курса.
Общи мерки
- Обездвижване/легло на седалката
- Кислород при хипоксемия SaO2 90 mmHg (предпазливост при систолично кръвно налягане 90–110 mmHg, противопоказано, ако има недостатъчна тъканна перфузия въпреки адекватен статус на пълнене
- Понякога незаменима, но като цяло много предпазлива употреба (повишен риск от аритмия, провокиране на исхемия), вероятно левосимендан вместо инотропи (MIPS).
Бета-блокери
- В острия стадий, посочен само в изключителни случаи (напр. Интравентрикуларна динамична обструкция)
- Внимание: Прилагането на бета-блокер за контрол на сърдечната честота (особено IV) без знание за функцията на ЛН може да утаи кардиогенен шок
- Съществуващата терапия с бета-блокери, ако е възможно, не се прекратява напълно, възможно е временно намаляване на дозата
Кардиоверсия/антиаритмици (вж. Конкретни глави)
- Електрическа кардиоверсия при пациенти с предсърдни или камерни аритмии, за които се смята, че са причина за остра сърдечна недостатъчност
- Антиаритмици: в допълнение към бета-блокерите, само амиодарон (Cordarone)
- Антиаритмици от клас IB/C, противопоказани при дисфункция на ЛН
Антикоагулация/инхибиране на тромбоцитната агрегация
- Остър коронарен синдром: в съответствие със стандарта (виж глава «Остър коронарен синдром» страница)
- Предсърдно мъждене/трептене: орална антикоагулация, хепарин (вж. Глава «Страница на предсърдно мъждене)
Опции за механична терапия
- Коронарография/PCI: ако се подозира, че причинителят е голяма миокардна исхемия
- Спешна операция ACBP (рядко)
- Спешна операция за механични инфарктни усложнения (разкъсване на папиларен мускул, дефект на вентрикуларна преграда, разкъсване на свободната стена)
- Спешна операция при усложнения от ендокардит
- IABP (противопоказан за аортна дисекция, значителна аортна регургитация): обикновено се използва в лабораторията за сърдечен катетър преди/след PCI при избрани пациенти
- Перкутанно устройство за подпомагане на лявата камера (LVAD): Impella, обикновено се използва в лабораторията за сърдечен катетър преди/след PCI при избрани пациенти
- VA-ECMO: за пациенти в кардиогенен шок, дори след реанимация, с относително кратко време без поток. Индикация предимно от екипа на MIPS, потърсете ранно обсъждане на индикацията (вижте страницата «Индикации за ECMO»)
- Хирургично ляво вентрикуларно асистиращо устройство: Дискусия със сърдечна хирургия
Диагноза
- Принцип на диагностика и алгоритъм вижте по-горе
- Ехокардиографията е основният образен инструмент; Сърдечният ЯМР често има смисъл и за първоначална диагноза (етиологично изясняване на кардиомиопатията, определяне на жизнеспособността при хронична ИБС)
- Коронарография: не е задължително показана за всяка новодиагностицирана сърдечна недостатъчност; ако етиологията е неясна в хода (не остра), но най-вече полезна
терапия
Когато е възможно, причинно-следствена терапия (лечение на исхемия и др.). В противен случай общи немедикаментозни мерки и лекарствена терапия, която е добре дефинирана за пациенти с HFrEF и слабо дефинирана за пациенти с HFpEF.
Немедикаментозни мерки (ако е възможно, обучение от медицински сестри със сърдечна недостатъчност)
- Общи мерки (обучение на пациенти и роднини, съвети за наркотици, диета, упражнения и социални навици) [1]
- Нормализиране на теглото
- Ограничен прием на сол
- Максимална консумация на алкохол (макс. 30 g/ден за мъже и 20 g/ден за жени); В случай на алкохолно-токсична кардиомиопатия, алкохолна абстиненция по принцип няма алкохол
- Редовни физически упражнения със стабилна сърдечна недостатъчност
Търсене на оптимизируеми съпътстващи заболявания
Несърдечно-съдови: анемия, белодробни заболявания, бъбречна дисфункция, дисфункция на щитовидната жлеза
Медикаментозна терапия за HFrEF
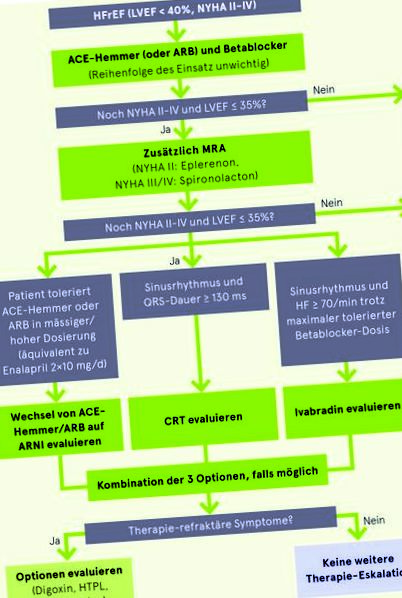
Терапията на хроничен HFrEF следва добре дефинирана стъпкова схема. В допълнение към симптоматичното лечение с бримкови диуретици, трябва да се установят трите основни камъка на терапията: АСЕ инхибитори (или антагонисти на ангиотензиновите рецептори, ARB), бета-блокери и блокери на минералокортикоидните рецептори (MRA), тогава има още три установени опции, които могат да се използват индивидуално (сакубитрил/Валсартан, ивабрадин, сърдечна ресинхронизация), след това опции за терапевтично рефрактерни ситуации (Фигура "Терапия HFrEF")
Диуретици
Диуретици с първичен цикъл (фуроземид, торасемид)
- Ефективен като симптоматична терапия за задържане на течности
- Оптимизиране на дозата чрез определяне и контролиране на „сухото тегло“, т.е. индивидуална доза
- Най-важните нежелани странични ефекти: хипокалиемия, хипомагнезиемия, хипонатриемия, нарушения на киселинно-алкалния баланс, хиперурикемия
- След достигане на еуволемия диуретиците трябва да бъдат намалени до необходимата минимална доза в полза на прогностично важните лекарства (АСЕ инхибитори, ARB, ARNI, бета-блокери, MRA) (диуретиците не подобряват прогнозата).
- С eGFR 2 не използвайте тиазидни диуретици, освен ако не се използва синергично с диуретици с контур.
- Ограничен прием на сол
- Неадекватен отговор: увеличете дозата на диуретик, евентуално предписвайте няколко пъти на ден, комбинирайте бримкови диуретици и метолазон (2,5 - 5 mg/ден) (последователна нефронова блокада), интравенозни бримкови диуретици (фуроземид) за чревна конгестия и намалена абсорбция (вж. Остра сърдечна недостатъчност).
АСЕ инхибитори
Първична основна терапия за всички пациенти с HFrEF (LVEF започва с ниски дози, увеличаване до поддържаща доза (удвояване на дозата на всеки 14 дни под контрол на калий и креатинин, целева доза според проучванията), възможно по-бързо титриране в болницата
Ангиотензин рецепторни блокери, ARB
Инхибитори на неприлизин на рецептора на ангиотензин (ARNI): в момента са налични само Sacutril/Valsartan
- Комбинация от ARB с инхибитор на неприлизин (инхибира разграждането на BNP и по този начин увеличава наличността на биологично активен BNP)
- Сакубитрил/валсартан превъзхожда АСЕ инхибитора еналаприл по отношение на намаляването на смъртността при пациенти, които са били на хронична терапия с АСЕ инхибитори или ARB
- Преобразуване на пациенти, приемащи АСЕ инхибитори (или ARB) и бета-блокери в оптимални дози и обикновено MRA и LVEF. Сърдечната ресинхронизация (CRT) е важна опция за терапия, която трябва да бъде проверена според алгоритъма. За подробности/специални ситуации вижте глава «ICD и CRT» страница.
Дигоксин
- Резервно лекарство, няма данни за подобряване на прогнозата
- Контрол на скоростта при пациенти с HFrEF и предсърдно мъждене
- Симптоматични пациенти (NYHA II - IV) с HFrEF в синусов ритъм въпреки оптималната терапия (според алгоритъма)
- Дозировка в зависимост от възрастта и бъбречната функция: 0,125 mg/ден, понякога само 3 ×/седмица
- Контрол на първоначалното ниво (максимум 0,8 ng/ml, не по-ефективен при по-високи нива, но токсичен)
Повече опций
- Желязо: интравенозното желязо (Fe-карбомалтоза) е опция за подобряване на симптомите при пациенти HFrEF, NYHA II/III, Hb 9,5–13,5 g и дефицит на желязо (феритин. На практика трябва да се изпробва от кои лекарства пациентът ще се възползва най-добре симптоматично.
- Важно:
- Избягване/лечение на тахиаритмии (предсърдно мъждене)
- Избягвайте изчерпването на обема и претоварването
Диуретици
Често е ефективен симптоматично. Пещера: тесен терапевтичен диапазон поради стръмна връзка между диастолното налягане и обема на лявата камера при задръстване на HFpEF (Пещера: изчерпване на обема)
Дигоксин
Възможност за контрол на скоростта при тахикардиално предсърдно мъждене, полза неясна при синусов ритъм
АСЕ инхибитори и ARB
Теоретично разумно (подобряване на релаксацията, намаляване на хипертрофията), полза, която не е доказана при пациенти с установено заболяване (т.е. не е профилактика) или няколко големи проучвания са отрицателни: вероятно въпреки това полезни при пациенти с хипертония.
Спиронолактон
Без ефект върху смъртността, но намаляване на риска от повторни хоспитализации и подобряване на ефективността, но повишен риск от бъбречна недостатъчност и хиперкалиемия; следователно използвайте разумно с внимателно проследяване на бъбречната функция и калия
Бета-блокери
Теоретично разумно (намаляване на сърдечната честота, удължаване на диастолата), но ситуацията с данни е неясна (ползата не е доказана)
Ивабрадин
Теоретично разумно (намаляване на сърдечната честота, удължаване на продължителността на диастолата). Ситуация с данни относно ефекта върху изпълнението противоречива; Може да се използва в избрани случаи
Блокери на калциевите канали (дихидропиридини)
Теоретично разумно (забавяне на сърдечната честота [Isoptin, Dilzem], подобряване на релаксацията), но няма данни за прогнозата. Употреба, но възможна (не е противопоказана за разлика от HFrEF)
Амиодарон
Контрол на ритъма в епизоди на предсърдно мъждене с последователни декомпенсации
PD Dr. Миха Мадер
Д-р Марк Бусер
Д-р Джан-Рето Клегер
Професор доктор. Ханс Рикли
Д-р Робърт Сийбър
- Сърдечно-съдово ръководство - PDF безплатно изтегляне
- Сърдечна недостатъчност (сърдечна недостатъчност); Ръководство за диабет
- Сърдечна недостатъчност (Сърдечна недостатъчност, Сърдечна недостатъчност) - Наблюдател
- Сърдечна недостатъчност mediX Швейцария
- Сърдечна недостатъчност при кучета Списанието за любителите на животните