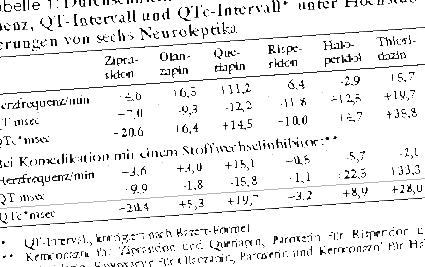ОТНОСНО НОВОТО ВЪВЕДЕНИЕ: ЗИРАЗИДОН (ZELDOX) НЕВРОЛЕПТИЧЕН
Зипразидон (ZELDOX), рекламиран като атипичен невролептик, също е на пазара в Германия от май. В САЩ одобрението първоначално беше отхвърлено през 1998 г. поради съображения за безопасност. След като лекарството беше одобрено при втория опит през 2001 г., предупредителните съобщения трябва да бъдат затегнати.1 Въпреки всичко, Pfizer рекламира продукта като "добре балансиран. Това се осигурява от многофакторния профил на толерантност"2 - нов критерий, създаден от маркетинга.
ОТНОСЕНИЯТА: Зипразидон в зависимост от дозата удължава това QT интервал в EKG. През 1998 г. FDA на САЩ не видя доказано предимство пред невролептиците, които вече са на пазара, което би надвишило повишения риск от потенциално фатални сърдечни аритмии. По това време FDA определи QTc * удължаване от 5 до 10 msec при максимални кръвни нива като достатъчно безопасно.3
Две години по-късно Pfizer представи на агенцията рандомизирано контролирано проучване, което сравнява ефекта на зипразидон върху QT интервала с този на пет други невролептици. Всички се титрират до максималната препоръчителна доза. Във втора фаза пациентите приемат и метаболитен инхибитор, който е специално избран за всеки невролептик. Преди началото на приложението и по време на пикови нива при монотерапия и комбинирана терапия, се записват ЕКГ. В проучването участват 183 пациенти. Двата агента с най-силно удължаване на QTc са тиоридазин (MELLERIL et al.; Средно 35,8 msec) и зипразидон (средно 20,6 msec; виж таблица 1). С увеличаване на сърдечната честота некоригираният QT интервал трябва да намалее. Със зипразидон и тиоридазин той се удължава въпреки увеличаването на сърдечната честота. Удължаването на QTc с повече от 75 msec се случва само с тиоридазин и зипразидон.3 Поради този риск тиоридазинът е понижен като лекарство от последен избор (a-t 2000; 31: 72).
Честотата на внезапна смърт също изглежда по-висока при зипразидон, отколкото при други невролептици, според данните от документите за одобрение на FDA (вж. Таблица 2). Още по-висок процент е документиран в това предпазливо интерпретирано ретроспективно сравнение само със сърдиндол (по-рано: SERDOLECT; a-t 1998; № 1: 19), който „катастрофира“ поради кардиотоксичност. Авторът на обзора на FDA за втори път се обявява против одобрението на зипразидон.3
ХАРАКТЕРИСТИКИ: Зипразидон няма химическа връзка с фенотиазини или бутирофенони. Той блокира както допаминовите D2, така и серотониновите 5НТ2 рецептори. Той също така инхибира хистамин Н1 и адренергичните алфа1 рецептори и обратното поемане на серотонин и норадреналин от синаптичната цепнатина.4.5 Зипразидон се абсорбира добре след поглъщане и се елиминира главно чрез метаболизма в черния дроб. CYP3A4 също участва в метаболизма. Изглежда, че два от основните метаболити имат QT удължаващ ефект.6-то
КЛИНИЧНА ЕФЕКТИВНОСТ: Според едно от малкото напълно публикувани проучвания, 40 mg и 80 mg зипразидон перорално два пъти дневно действат по-добре от плацебо при 302 пациенти с остро обостряне на шизофренична психоза или шизоафективно заболяване в продължение на шест седмици.7-ми В проучване с 139 пациенти само дневната доза от 60 mg два пъти в продължение на четири седмици има значително предимство пред плацебо в две от трите първични крайни точки, но не и дозата от 20 mg два пъти, препоръчана за поддържаща терапия.8 пациенти с терапевтична резистентност и съответна ЕКГ Промените са изключени от двете проучвания. Друго по-малко проучване с 90 пациенти, при което са сравнени няколко дози зипразидон от 4 mg дневно до 160 mg дневно с 15 mg халоперидол (HALDOL и др.), Също не подкрепя принципа на лечение. По отношение на първичната крайна точка, няма разлика между по-високата и най-ниската доза на зипразидон.3.9
Проучвания за подготовка на IM,10-12 което все още не е одобрено в САЩ поради съображения за безопасност,13 са недостатъчно информативни поради методологически недостатъци. Необходимостта от парентерално лечение не може да се разбере въз основа на критериите за включване и валидността на едно на две проучвания10.11 Не проверявайте използваната скала за измерване. Едно предимство пред халоперидол е директното сравнение поради отворен дизайн12 не е адекватно документиран.
НЕЖЕЛАНИ ЕФЕКТИ: Най-честият нежелан ефект след перорален прием е сънливост. 1% до 10% от пациентите се оплакват от главоболие, замаяност, зрителни нарушения, ортостатична хипотония и тахикардия, стомашно-чревни разстройства като гадене и повръщане, кожен обрив (5%), екстрапирамидни симптоми (5%), акатизия (8%) и дистония (4%).5.6 След IM инжекции болката в областта на инжектирането също е често срещана.14-ти Понякога са описани синкоп, гърчове и повишен пролактин.5.6 Според предишния опит наддаването на тегло изглежда по-малко при зипразидон, отколкото при други невролептици.2 В краткосрочни проучвания обаче 10% повече пациенти със зипразидон наддават поне 7% телесно тегло, отколкото с фиктивно лекарство (4%).5
Зипразидон не трябва да се използва, ако се знае, че QT интервалът се удължава след остър миокарден инфаркт, при некомпенсирана сърдечна недостатъчност или сърдечни аритмии. Едновременната употреба на QT-удължаващи лекарства като антиаритмици или антималарийни лекарства като халофантрин (HALFAN) е противопоказана. Инхибиторът на CYP-3A4 кетоконазол (NIZORAL) повишава серумните нива на зипразидон и неговите метаболити, но изглежда няма ефект върху удължаването на QT интервала (Таблица 1).5.6
ДОЗА И РАЗХОДИ: За поддържаща доза от 40 mg зипразидон (ZELDOX) два пъти дневно, 230 евро на месец е четиринадесет пъти по-висока от цената на 10 mg халоперидол (HALDOL: 17 евро/месец; ХАЛОПЕРИДОЛ ДЕСИТИН: 16 евро/месец).
ЗАКЛЮЧЕНИЕ: Невролептичният зипразидон (ZELDOX) изглежда е по-кардиотоксичен от другите невролептици, според данните, предоставени на FDA на САЩ. Не виждаме предимство, което би надхвърлило повишения риск от непредвидими, тежки сърдечни аритмии и внезапна сърдечна смърт, и следователно причина, която би оправдала одобрението. Няма клинични доказателства за "атипични" свойства, по-специално за ползата при пациенти, които не се повлияват от конвенционалната терапия и за по-нисък риск от тардивна дискинезия.
Тази публикация е защитена с авторски права. Дублирането, както и запазването и обработката в електронни системи е разрешено само с одобрението на arznei-telegram ®.
- БЕЗОПАСНОСТ НА ЛЕКАРСТВАТА И VIAGRA - телеграма за наркотици
- CANNABINOID-1-BLOCKER RIMONABANT (ACOMPLIA) ЗА НАМАЛЯВАНЕ НА ТЕГЛОТО - arznei telegram
- A VOTRE SANT; АЛКОХОЛ И КРЪВНИ ЛИПИДИ - лекарствена телеграма
- АНТИЕПИЛЕПТИКА НОВА СРЕЩУ СТАРОТЕСТИРАНА - телеграма arznei
- Атипичен невролептичен зипразидон нови възможности за лечение на Sch