Действието на инсулина в мозъка може да доведе до затлъстяване
Изследователите дешифрират важен механизъм, чрез който инсулинът контролира енергийния баланс в хипоталамуса
Мазните храни ви напълняват. Тази проста връзка крие сложни сигнални пътища, чрез които пратените вещества в мозъка контролират енергийния баланс. Учени от Института за неврологични изследвания Макс Планк в Кьолн и Клъстера за върхови постижения CECAD към Университета в Кьолн сега изясниха важна стъпка в тази сложна верига за контрол. Те успяха да покажат как хормонът инсулин действа в така наречения вентромедиален хипоталамус на мозъка. Инсулинът се отделя в по-голяма степен в резултат на диета с високо съдържание на мазнини. В специални нервни клетки - SF-1 невроните - той задейства сигнална каскада в движение, в центъра на която е ензимът PI3-киназа. В няколко междинни стъпки инсулинът инхибира предаването на нервни импулси по такъв начин, че чувството за ситост да бъде потиснато и консумацията на енергия да бъде намалена. Това насърчава наднорменото тегло и затлъстяването.
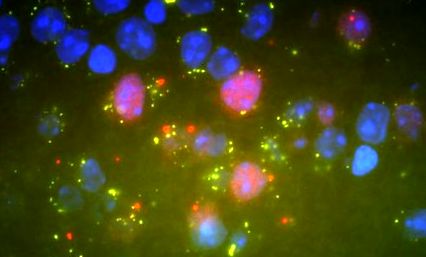
Визуализация на ефектите на инсулина в SF-1 невроните на хипоталамуса. След стимулация с инсулин, клетките SF-1 (червени) образуват сигналната молекула PiP3 (зелено). (Синьо: клетъчно ядро)
Хипоталамусът играе важна роля в регулирането на енергийния баланс. Специални нервни клетки в тази област, така наречените POMC клетки, реагират на пратените вещества и по този начин контролират хранителното поведение и консумацията на енергия. Хормонът инсулин е важно пратено вещество. В организма инсулинът има ефект, че абсорбираната чрез храната захар се транспортира до целевите клетки (напр. Мускулите) и по този начин е на разположение като енергиен източник. При диета с високо съдържание на мазнини тя все повече се образува в панкреаса, така че концентрацията му в мозъка също се увеличава. Взаимодействието между инсулина и целевите клетки в мозъка също е от решаващо значение за контрола и регулирането на енергийния баланс. Молекулните механизми, залегнали в основата на контрола от инсулина, все още са до голяма степен неизвестни.
Изследователска група, ръководена от Йенс Брюнинг, директор на Института за неврологични изследвания „Макс Планк“ и ръководител на клъстера за върхови постижения CECAD („Отговорите на клетъчния стрес при заболявания, свързани със стареенето“) в университета в Кьолн, сега изясни важна стъпка в този сложен набор от правила. Както учените показаха, инсулинът задейства сигнална каскада в SF-1 невроните - друга група нервни клетки в хипоталамуса. Интересното е обаче, че тези клетки изглежда се регулират от инсулина само при диета с високо съдържание на мазнини и наднормено тегло. Ензимът PI3-киназа играе централна роля в тази каскада от пратеници на вещества. Ензимът активира йонните канали чрез междинни етапи и по този начин инхибира предаването на нервни импулси. Изследователите подозират, че по този начин SF-1 клетките комуникират с POMC клетките.
Киназите са ензими, които активират други молекули чрез фосфорилиране - свързването на фосфатни групи. „Ако инсулинът се свърже със своя рецептор на повърхността на SF-1 клетките, той активира PI3 киназата“, обяснява Тим Кльокенер, първи автор на изследването. „PI3 киназата от своя страна контролира образуването на PIP3, друга сигнална молекула, чрез фосфорилиране. PIP3 прави съответните канали в клетъчната стена пропускливи за калиеви йони. ”Притокът им кара нервната клетка да„ стреля ”по-бавно - потискането на електрическите импулси.
„Ако SF-1 невроните са между тях, тогава инсулинът вероятно индиректно инхибира POMC невроните, които са отговорни за чувството за ситост, ако имате наднормено тегло“, подозира ученият. „В същото време приемът на храна продължава да се увеличава.“ Пряко доказателство обаче, че двата типа нервни клетки комуникират директно помежду си по този начин, все още се чака.
За да разберат как действа инсулинът в мозъка, учените от Кьолн сравняват мишки, на които липсва инсулиновият рецептор на SF-1 невроните, с мишки, чийто инсулинов рецептор е непокътнат. При нормална диета изследователите не откриха разлика между двете групи. Това предполага, че инсулинът няма решаващо влияние върху активността на тези клетки при слаби индивиди. Ако, от друга страна, гризачите са били хранени с диета с високо съдържание на мазнини, тези с дефектен инсулинов рецептор остават слаби, докато тези с функциониращ рецептор бързо напълняват. Както повишеният апетит, така и намалената консумация на калории са отговорни за увеличаването на теглото. Този ефект на инсулина може да представлява еволюционна адаптация на организма към нередовно снабдяване с храна с дълги периоди на глад: Ако има краткосрочно прекомерно предлагане на особено богата на мазнини храна, тялото може да създаде енергийни резерви особено ефективно чрез действието на инсулина.
Все още не е възможно да се прецени дали резултатите от изследването ще помогнат един ден да се намеси конкретно в енергийния баланс. „В момента все още сме далеч от практическото приложение“, казва Йенс Брюнинг. „Нашата цел е да разберем как възникват гладът и ситостта. Едва когато разберем цялата система, можем да започнем да разработваме терапии. "
- Диетата или неправилното хранене могат да доведат до загуба на мускулна маса
- Задръстете 10 вещества, които програмират мозъка да бъде затлъстял
- В мозъка се появява болезнено затлъстяване
- Krass защо диетичната сода може да увреди здравето на мозъка ви
- Ново проучване разкрива, че твърде много чили в храната може да доведе до здраве на деменция